W 2016 roku Yoshinori Ohsumi otrzymał Nagrodę Nobla w dziedzinie fizjologii i medycyny za odkrycie mechanizmów autofagii – procesu, który od tamtej pory elektryzuje zarówno środowisko naukowe, jak i miliony ludzi szukających naturalnych metod wspierania zdrowia. Post, ograniczenie kalorii, aktywność fizyczna – to narzędzia, które mogą uruchomić w komórkach coś w rodzaju wewnętrznego programu sprzątającego. Ale jak naprawdę działa autofagia, kiedy faktycznie się włącza i czy można jej nadużyć? Oto, co naprawdę mówi nauka.
W skrócie – 3 rzeczy, które warto wiedzieć:
- Autofagia to nie moda, lecz ewolucyjnie stary mechanizm – komórki „zjadają” swoje uszkodzone składniki, by odzyskać energię i materiał budulcowy. Działa non stop, ale dopiero w warunkach ograniczonego dostępu do energii – jak podczas postu – wyraźnie przyspiesza.
- Nie ma jednego „złotego progu” aktywacji – badania wskazują, że autofagia nasila się między 16 a 48 godziną postu, ale dokładny moment zależy od metabolizmu, poziomu glikogenu, aktywności fizycznej i indywidualnych cech organizmu.
- Autofagia ma dwa oblicza – nadmiernie lub niekontrolowanie aktywowana może sprzyjać przeżyciu komórek nowotworowych. To nie jest mechanizm, który zawsze „naprawia” – to narzędzie, które działa w kontekście.
Spis treści
Czym właściwie jest autofagia i dlaczego dostała Nobla?
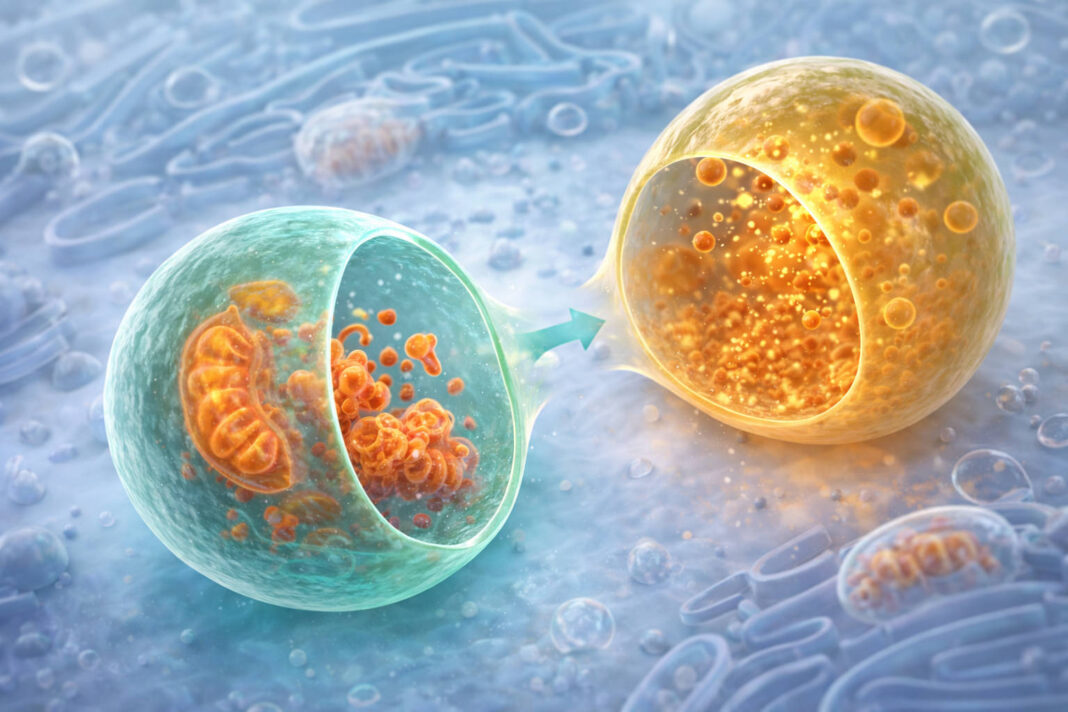
Słowo „autofagia” pochodzi z greki: autos (sam) i phagein (jeść). Dosłownie: samozjadanie. Brzmi nieprzyjemnie, ale to jeden z najbardziej eleganckich procesów biologicznych, jakie wykształciła ewolucja.
Kiedy komórka jest zagrożona – brakuje energii, nakumulowały się uszkodzone białka albo do wnętrza przedostał się patogen – uruchamia wewnętrzny program recyklingu. Tworzy się specjalna dwubłonowa struktura, zwana autofagosomem, która dosłownie otacza to, co należy usunąć: wadliwe mitochondria, zniszczone białka, fragmenty błon komórkowych, a nawet bakterie czy wirusy. Autofagosom łączy się następnie z lizosomem – „trawiennym woreczkiem” komórki – gdzie cała zawartość zostaje rozłożona na proste składniki i ponownie wykorzystana.
Przez dekady biologom brakowało narzędzi, by ten proces dokładnie zbadać. Zmienił to Yoshinori Ohsumi, który w latach 90. zidentyfikował u drożdży geny odpowiedzialne za autofagię – tzw. geny ATG (autophagy-related genes). Okazało się, że ich odpowiedniki istnieją niemal identycznie u ssaków, w tym u człowieka. To odkrycie otworzyło zupełnie nowe pole badań i przełożyło się na zrozumienie dziesiątek chorób.
Ludzki genom zawiera ponad 40 genów bezpośrednio związanych z autofagią. Mutacje w niektórych z nich zostały powiązane z chorobą Parkinsona, Crohna, cukrzycą typu 2 i nowotworami – co pokazuje, jak fundamentalna jest ta funkcja dla zdrowia całego organizmu. (Khandia i wsp., 2019)
Dziś wiemy, że autofagia pełni co najmniej kilka kluczowych ról:
- utrzymuje jakość wewnętrznych składników komórki (tzw. kontrola jakości białek i organelli),
- uczestniczy w obronie przeciwinfekcyjnej – ksenofagia to selektywne usuwanie patogenów wewnątrzkomórkowych,
- reguluje odpowiedź na stres metaboliczny,
- odgrywa rolę w embriogenezie i różnicowaniu komórek,
- wpływa na tempo procesów starzenia.
Kiedy autofagia się włącza? Molekularny „czujnik głodu”
W organizmie stale odżywianym autofagia działa na minimalnym, podstawowym poziomie – utrzymuje porządek, ale nie pędzi. Dopiero wyraźny sygnał niedoboru energii przestawia komórkę w tryb intensywnego recyklingu.
Kluczową rolę pełnią tutaj dwa szlaki sygnalizacyjne:
AMPK (AMP-activated protein kinase) – enzym działający jak czujnik poziomu paliwa. Kiedy stosunek AMP do ATP w komórce rośnie (czyli energia spada), AMPK się aktywuje i uruchamia procesy oszczędnościowe, w tym autofagię. Bada to m.in. Gregory Steinberg, który wykazał, że AMPK pełni rolę strażnika metabolizmu mitochondrialnego.
mTOR (mechanistic target of rapamycin) – działa odwrotnie. To sensor dostępności składników odżywczych i aminokwasów. Gdy mTOR jest aktywny (bo jest dużo jedzenia), hamuje autofagię. Gdy jest nieaktywny – autofagia rusza pełną parą.
Innymi słowy: insulina i glukoza włączają mTOR i blokują autofagię. Post i aktywność fizyczna obniżają mTOR i uruchamiają AMPK – co razem daje sygnał do komórkowego „generalnego remontu”.
Ile czasu zajmuje ta aktywacja? Tu nauka nie daje jednej odpowiedzi. Dostępne badania wskazują, że wyraźne nasilenie autofagii następuje między 16 a 24 godziną postu, choć część badaczy obserwuje istotne zmiany dopiero po 24–36 godzinach. Szczyt aktywności przy dłuższych postach (48–72 h) jest dobrze udokumentowany w badaniach na modelach zwierzęcych, natomiast bezpośrednie pomiary u ludzi są znacznie trudniejsze metodologicznie i wciąż ograniczone.
Post przerywany, przedłużony i ograniczenie kaloryczne – co aktywuje autofagię skuteczniej?
Post przerywany (Intermittent Fasting)
Najbardziej popularny model to 16:8 – 16 godzin bez jedzenia, 8-godzinne okno żywieniowe. Dla większości osób oznacza to po prostu rezygnację ze śniadania lub późnej kolacji. To nie jest „post głęboki” – autofagia wchodzi na wyższy bieg, ale nie osiąga szczytowych wartości. Niemniej regularne stosowanie tego modelu wiąże się z poprawą wrażliwości insulinowej, redukcją markerów zapalnych i lepszą regulacją glikemii – co pośrednio tworzy środowisko sprzyjające efektywniejszej autofagii.
Inne protokoły – jak 5:2 (dwa dni z bardzo niską podażą kaloryczną w tygodniu) czy OMAD (jeden posiłek dziennie) – są intensywniejsze i mogą głębiej aktywować szlaki autofagiczne, ale wymagają większej ostrożności i adaptacji organizmu.
Post przedłużony (24–72 godziny)
To tu autofagia osiąga poziomy dobrze mierzalne nawet w badaniach klinicznych. Valter Longo z University of Southern California jest jednym z czołowych badaczy w tej dziedzinie – jego prace nad postami 3–5-dniowymi (i ich naśladowczynią, Fasting Mimicking Diet) wykazały korzystne zmiany w markerach zapalnych, poziomie IGF-1 i biomarkerach biologicznego wieku.
Jednak post powyżej 24 godzin to poważna interwencja metaboliczna, która bez odpowiedniego przygotowania i nadzoru niesie realne ryzyko – szczególnie dla osób z cukrzycą, chorobami serca, nerek, tarczycy oraz kobiet w ciąży i karmiących.
Ograniczenie kaloryczne (Caloric Restriction)
Redukcja codziennej podaży kalorii o 20–30% bez konkretnych okien postnych – klasyczna strategia badana w kontekście długowieczności od lat 30. XX wieku. Aktywuje autofagię łagodniej, ale konsekwentnie. Trudna do stosowania długoterminowo ze względu na presję społeczną i biologiczne mechanizmy kompensacyjne (wzrost apetytu).
Ćwiczenia fizyczne – niedoceniany aktywator autofagii
Post to nie jedyna droga. Regularna aktywność fizyczna – zarówno aerobowa, jak i siłowa – aktywuje AMPK w mięśniach szkieletowych i stymuluje autofagię niezależnie od ograniczeń żywieniowych.
Przełomowe badania Noboru Mizushimy i zespołu He i wsp. opublikowane w Nature wykazały, że intensywny wysiłek fizyczny wyraźnie nasila autofagię w mięśniach – a myszy z genetycznie zablokowaną autofagią traciły sprawność mięśniową szybciej i wykazywały gorszą tolerancję wysiłku. U ludzi analogiczne obserwacje potwierdzono pośrednio przez pomiary biomarkerów.
Co istotne, ćwiczenia i post mogą działać synergicznie – aktywność fizyczna w stanie lekkiego deficytu energetycznego (np. trening cardio rano, przed pierwszym posiłkiem) to jeden z bardziej efektywnych sposobów na pogłębienie sygnałów autofagicznych bez konieczności stosowania wielodniowych głodówek.
Dieta i związki bioaktywne – co mówi nauka o „aktywatorach” autofagii?
Internet roi się od suplementów reklamowanych jako „aktywatory autofagii”. Warto być wobec nich ostrożnym, bo większość danych pochodzi z badań in vitro lub na modelach zwierzęcych.
| Substancja | Źródło | Mechanizm | Status badań u ludzi |
|---|---|---|---|
| Spermidyna | Pszenica pełnoziarnista, sery dojrzewające, soja, grzyby | Aktywacja autofagii przez szlak hipusynylacji | Obiecujące próby kliniczne (pamięć u seniorów) |
| Resweratrol | Winogrona, borówki, orzeszki ziemne | Aktywacja sirtuin (SIRT1), pośrednia stymulacja autofagii | Głównie in vitro i zwierzęta; brak mocnych danych u ludzi |
| Kurkumina | Kurkuma | Hamowanie mTOR, działanie przeciwzapalne | Dane przedkliniczne; niska biodostępność problemem |
| EGCG | Zielona herbata | Modulacja szlaków PI3K/mTOR | Wstępne dane kliniczne, wymaga potwierdzenia |
| Rapamycyna | Syntetyczny inhibitor mTOR | Bezpośrednie hamowanie mTOR | Tylko w warunkach klinicznych (lek, nie suplement) |
Ważna uwaga: Żaden z powyższych suplementów nie zastąpi postu ani wysiłku fizycznego jako aktywatora autofagii u zdrowego człowieka. Mechanizmy działające in vitro nie przekładają się automatycznie na efekty kliniczne – i jest to jeden z najczęstszych błędów komunikacyjnych w popularyzacji tego tematu.
Co hamuje autofagię? Czynniki, o których rzadko się mówi
Skoro tak wiele rzeczy może autofagię wspierać, warto wiedzieć, co ją konsekwentnie wygasza:
Wysoka podaż białka i węglowodanów prostych aktywuje mTOR i blokuje autofagię – efektywnie nawet po kilkugodzinnym poście. Dlatego posiłek bogaty w białko tuż przed oknem postnym może znacząco skrócić efektywny czas jego działania.
Przewlekły stres i wysoki kortyzol zaburzają gospodarkę insulinową i osłabiają sygnały autofagiczne. To paradoks: wiele osób próbuje aktywować autofagię postem, jednocześnie żyjąc w chronicznym stresie, który blokuje jej efekty.
Niedobór i nieregularność snu – rytm cyrkadianowy ma bezpośredni wpływ na ekspresję genów ATG. Badania wskazują, że szczytowa aktywność autofagii w wielu tkankach przypada na konkretne fazy nocne. Nieregularne godziny snu lub jego chroniczny niedobór zakłócają ten cykl.
Alkohol i dym tytoniowy zaburzają przede wszystkim selektywną autofagię – mitofagię (usuwanie uszkodzonych mitochondriów) i ksenofagię.
Autofagia a choroby – co naprawdę wiemy?
Choroby neurodegeneracyjne
W chorobie Parkinsona i Alzheimera obserwuje się wyraźne upośledzenie autofagii – co prowadzi do akumulacji toksycznych agregatów białkowych (alfa-synukleiny, tau, amyloidu-β). Przywrócenie sprawności tego procesu jest aktywnie badane jako cel terapeutyczny. Wstępne badania kliniczne nad spermidyną u seniorów (Wirth i wsp.) wykazały poprawę markerów pamięci, ale badania są jeszcze we wczesnej fazie.
Nowotwory – złożona i dwuznaczna rola
To jeden z najważniejszych i najczęściej pomijanych aspektów. Autofagia nie jest prosta w kontekście raka. W zdrowych komórkach hamuje inicjację nowotworową – usuwa uszkodzone elementy, zanim staną się źródłem mutacji. Ale w komórkach nowotworowych, które już istnieją, autofagia może pomagać im przeżyć w warunkach niedotlenienia i niedoboru składników odżywczych – czyli dokładnie w warunkach guza.
Stąd prowadzone są badania kliniczne zarówno nad aktywatorami (w profilaktyce), jak i inhibitorami autofagii (w leczeniu istniejących nowotworów – np. hydroksychlorochina w skojarzeniu z chemioterapią). Uproszczone hasło „post leczy raka” jest nie tylko naukowym nadużyciem – może być niebezpieczne.
Choroby metaboliczne
Insulin resistance, cukrzyca typu 2, niealkoholowe stłuszczenie wątroby – we wszystkich tych schorzeniach obserwuje się upośledzoną autofagię. Poprawę autofagii jako mechanizm korzystnego działania postu przerywanego dokumentuje coraz więcej badań, choć związki przyczynowo-skutkowe u ludzi wymagają dalszego potwierdzenia.
Dla kogo post jest bezpieczny, a kto powinien uważać?
To pytanie jest fundamentalne i zbyt często pomijane w popularnych artykułach o autofagii.
Bez konsultacji lekarskiej, zdrowa dorosła osoba może bezpiecznie:
- wprowadzić codzienne okno żywieniowe 12–16 godzin,
- wzbogacić dietę w naturalnie bogate w spermidynę produkty (pełne ziarno, nasiona, dojrzałe sery, kiełki pszenicy),
- regularnie ćwiczyć (minimum 150 minut umiarkowanej aktywności tygodniowo),
- zadbać o regularność snu i ograniczyć jedzenie w późnych godzinach wieczornych.
Konsultacja z lekarzem jest konieczna przed wprowadzeniem jakichkolwiek protokołów postnych, jeśli:
- chorujesz na cukrzycę (zwłaszcza leczoną insuliną lub lekami doustnymi),
- masz choroby serca, nerek lub tarczycy,
- przyjmujesz leki przewlekle (szczególnie immunosupresyjne, antykoagulanty),
- jesteś w ciąży lub karmisz piersią,
- masz historię zaburzeń odżywiania (anoreksja, bulimia, BED),
- jesteś dzieckiem lub nastolatkiem.
Najpopularniejsze mity o autofagii – weryfikacja
„Po 72 godzinach post działa najlepiej” – prawdą jest, że dłuższe posty aktywują autofagię głębiej, ale ryzyko rośnie proporcjonalnie, a efekty u ludzi (w przeciwieństwie do myszy) nie są tak jednoznaczne.
„Czarna kawa przerywa post i blokuje autofagię” – dostępne dane nie potwierdzają tego w przypadku czarnej kawy bez dodatków. Kofeina może wręcz wspierać aktywację AMPK. Kawa z mlekiem, syropem lub cukrem – owszem, może zaburzyć okno postne.
„Suplementy dają te same efekty co post” – fałsz. Mechanizmy in vitro nie przekładają się automatycznie na efekty u zdrowego człowieka w standardowych dawkach suplementacyjnych.
„Autofagia odmładza” – to duże uproszczenie. Autofagia usuwa uszkodzone elementy komórkowe i spowalnia pewne aspekty starzenia komórkowego, ale nie jest lekiem na starzenie się jako takie. Badania na modelach zwierzęcych są obiecujące; twarde dane kliniczne u ludzi są wciąż ograniczone.
Co nas czeka – kierunki badań
Nauka o autofagii jest wciąż młoda, a najciekawsze wyniki mogą dopiero nadejść. Kilka obszarów wygląda szczególnie obiecująco:
Badania nad spermidyną jako gerontoprotekcyjnym suplementem są obecnie w toku w kilku ośrodkach europejskich. Projekt TAME (Targeting Aging with Metformin) bada, czy metformina – aktywująca AMPK – może opóźniać biologiczne procesy starzenia. Rozwijają się też prace nad biomarkerami autofagii we krwi, które mogłyby umożliwić jej nieinwazyjny pomiar – co dramatycznie usprawniłoby badania kliniczne.
Równocześnie w onkologii trwają próby kliniczne z inhibitorami autofagii – wyniki badań fazy II/III z hydroksychlorochiną w różnych typach nowotworów mają szansę zmienić standardy leczenia.
Autofagia bez tajemnic – to, co warto zapamiętać
Autofagia to jeden z najbardziej fascynujących biologicznych mechanizmów, jakie znamy – i jeden z lepiej udokumentowanych sposobów, w jakie organizm radzi sobie z własnym starzeniem i uszkodzeniami. Post, aktywność fizyczna, jakościowy sen i dieta bogata w naturalne związki bioaktywne tworzą środowisko, w którym ten mechanizm działa sprawniej.
Ale to nie jest magiczny przełącznik. To złożony proces zależny od kontekstu, indywidualnego metabolizmu i stanu zdrowia. Najlepsza autofagia to ta, którą wspiera regularny, zrównoważony styl życia – a nie jednorazowe ekstremalne głodówki połączone z resztą dnia pełnego stresu, słabego snu i wysoko przetworzonej żywności.
Nauka dostarcza narzędzi. Zdrowy rozsądek decyduje, jak je stosować.
Źródła
- Ohsumi Y. Molecular dissection of autophagy: two ubiquitin-like systems. Nature Reviews Molecular Cell Biology, 2001. https://doi.org/10.1038/35052054
- Mizushima N., Levine B., Cuervo A.M., Klionsky D.J. Autophagy fights disease through cellular self-digestion. Nature, 2008; 451:1069–1075. https://doi.org/10.1038/nature06639
- He C., Bassik M.C., Moresi V. i wsp. Exercise-induced BCL2-regulated autophagy is required for muscle glucose homeostasis. Nature, 2012; 481:511–515. https://doi.org/10.1038/nature10758
- Steinberg G.R., Hardie D.G. New insights into activation and function of the AMPK. Nature Reviews Molecular Cell Biology, 2022. https://doi.org/10.1038/s41580-022-00547-x
- Longo V.D., Panda S. Fasting, Circadian Rhythms, and Time-Restricted Feeding in Healthy Lifespan. Cell Metabolism, 2016; 23(6):1048–1059. https://doi.org/10.1016/j.cmet.2016.06.001
- Madeo F., Carmona-Gutierrez D., Kepp O., Kroemer G. Spermidine delays aging in humans. Aging, 2018; 10(8):2209–2211. https://doi.org/10.18632/aging.101517
- Shabkhizan R. i wsp. The Beneficial and Adverse Effects of Autophagic Response to Caloric Restriction and Fasting. Biomedicine & Pharmacotherapy, 2023; 165:115271. https://doi.org/10.1016/j.biopha.2023.115271
- Khandia R. i wsp. A Comprehensive Review of Autophagy and Its Various Roles in Infectious, Non-Infectious, and Lifestyle Diseases. Cells, 2019; 8(7):674. https://doi.org/10.3390/cells8070674
- Liu S. i wsp. Autophagy: Regulator of cell death. Cell Death & Disease, 2023; 14:648. https://doi.org/10.1038/s41419-023-06154-8
- Boccardi V. i wsp. The potential of fasting-mimicking diet as a preventive and curative strategy for Alzheimer’s disease. International Journal of Molecular Sciences, 2023; 24(14):11291. https://doi.org/10.3390/ijms241411291
Artykuł ma charakter wyłącznie edukacyjny i nie stanowi porady medycznej. Przed wprowadzeniem jakichkolwiek protokołów postnych lub zmian w diecie skonsultuj się z lekarzem lub dietetykiem klinicznym.